Od začátku pandemie jsme byli ujištěni, že dodržování komunitního maskování vyřeší naše problémy a zastaví šíření SARS-CoV-2. Přesto data aplikací v reálném světě neustále ukazovala, že selhávají jako zmírňující opatření pro osobní ochranu, a místo abychom opravili kurz nahodilých pokynů, které byly vydány, bylo nám řečeno, abychom maska těžší se stále více omezujícími, i když účinně nezmírňujícími aparáty.
Ale proč selhali a proč selhávají i nadále? Níže se ponoříme do podrobností o tom, proč, i když předpokládáme hypotetickou dokonalou kapacitu zachycení, N95 nedokážou zmírnit šíření SARS-CoV-2.
Měli bychom začít tím, že se na virovou přenositelnost a produkci infekční hmoty budeme dívat jako na spektrum, založené na závažnosti onemocnění, imunitní odpovědi daného jedince a pokroku v průběhu nemoci. U všech bylo prokázáno, že mají významný dopad na virovou zátěž jedince infikovaného SARS-CoV-2. Budeme diskutovat výstupní hodnoty versus míry infekčnosti a metody měření minimální infekční dávky.
Každý z těchto důležitých faktorů je třeba vzít v úvahu při zmírňování patogenů i nezávisle, ale v kombinaci nám mohou konkrétně ukázat, zda daný přístup bude mít požadovaný výsledek při eliminaci infekčního nebezpečí. Výstupní hodnoty respiračních emisí ukazují, kolik hmoty je vylučováno jednotlivcem a zda jsou nebo nejsou přenosné respiračním patogenem, ale výstupní údaje se velmi liší mezi závažnějšími stádii nástupu nemoci, obdobími zotavení a když je PCR negativní. pro daný patogen.
Porovnáním výstupu s poměrem částice a jednotky tvořící plak (PFU) dostáváme míru toho, kolik emitovaných částic je životaschopných virionů schopných způsobit infekci. Každá z těchto infekčních jednotek je označována jako PFU. Počet PFU požadovaných k přijetí potenciálním hostitelem je dán jako údaj o minimální infekční dávce (MID), což je práh, který jakmile je splněn, je třeba očekávat nástup infekce.
Když se podíváme na údaje o poměru částic k PFU a vypočítáme potenciál MID, konečným produktem je potenciální počet jedinců, kteří mohou být infikováni za dané časové období.
S tímto prahem MID pro potenciál infekčnosti pak můžeme použít hypotetickou dokonalou kapacitu zachycení daného zařízení, abychom zjistili, zda nejlepší scénář povede k pravděpodobnosti, že zařízení zmírní nebo zabrání dosažení prahu MID pro dané nebezpečí.
Zde se podíváme na výstup, poměr částic k PFU a MID pro SARS-CoV-2 oproti hypotetické dokonalé záchytné kapacitě pro N95, abychom prokázali, že i při dokonalé rychlosti záchytu (a v tomto případě látky mnohem menší, než je zařízení schváleno nebo navrženo k zachycení), těch 5 % procent, které se nikdy nezachytí, je stále dostatečné množství potenciálního vystavení infekční látce, aby vedlo k infekci.
Rozsahy částic a odpovídající chování emitované hmoty
Opatření ke zmírnění pandemie měla začít s minimální životaschopnou velikostí částic, která u SARS-CoV-2 klesá na 0.06-0.14 µm. I když jsou N95 často tlačeny úředníky veřejného zdraví, jsou určeny a schváleny výhradně pro zachycení hmoty větší než 0.3 µm. Bylo prokázáno, že více než 90 % procent vydechovaných částic klesá pod 0.3 um. Tato velikost hmoty zůstává ve vzduchu po delší dobu — hodiny, dokonce dny, v závislosti na směnných kurzech vzduchu v daném prostoru. Ukázalo se, že SARS-CoV-2 zůstává životaschopný i po hodinách jako aerosol mimo hostitele a několik dní na površích.
"SARS-CoV-2 virus byl pozorován být životaschopný po dobu 3 hodin. v aerosolech, s poklesem koncentrace infekčního viru z 103.5 na 102.7 TCID50 na litr vzduchu."
Tato studie používala aerosoly vytvořené v laboratoři obsahující infekční SARS-CoV-2 a pozorovala životaschopnost emitovaných látek na různých površích a jako aerosoly v průběhu času.
Při zvažování následujících věcí si také klademe otázku, zda porézní masky a membrány respirátoru hrály roli při zvyšování doby životaschopnosti virové hmoty:
"Doba přežití vzdušných virů na površích lišit na základě zda jsou povrchy neporézní (např. plast, nerezová ocel, sklo) nebo porézní (např. papíry a oblečení). Neporézní povrchy jsou hlavním přispěvatelem k přenosu nemocí, protože bylo pozorováno, že doba přežití vzdušných virů na nich je mnohem delší než na porézních površích.
Masky a respirátory se jistě počítají jako porézní povrchy. Mnoho respirátorů je také vyrobeno z plastů vyfukovaných z taveniny. Byla v dostatečné míře studována životaschopnost virů na membránách masek?
Míra životaschopnosti aerosolu je důležitá, protože demonstruje schopnost přenosu v uzavřených prostorech bez přítomnosti přenosného jedince. S přenosný jedinec přítomný a vyzařující do daného prostoru by byl výstup konstantní a životaschopná virová hmota by zvyšovala saturaci atmosféry patogenem na základě jednoho dechu.
Přehlíženým, ale kritickým problémem u masek a respirátorů je těsnění – malé mezery způsobují, že tyto přístroje jsou pro nositele neúčinné. Málokdy, pokud vůbec, někdo nosí tyto přístroje správně, za nezbytných podmínek opotřebení, takže se setkáváme s nesprávným nošením již nezmírňujících přístrojů.
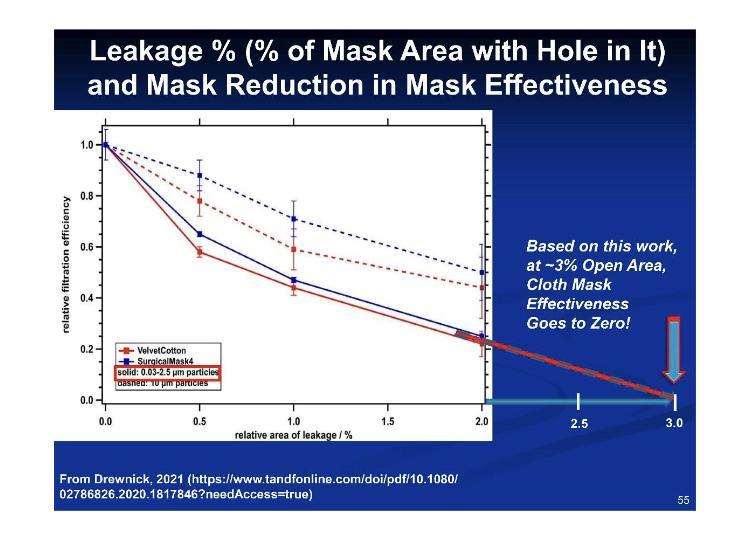
Podle těchto údajů pro lícování versus netěsnost se 3.2% procento úniku rovná 100% neúčinnosti.
To vše jsou faktory, které je třeba vzít v úvahu při řešení příčiny selhání přístroje při zmírnění daného nebezpečí. Dalším zkoumáním výstupu emisí, minimální infekční dávky, jednotek vytvářejících plak a jejich vztahu můžeme lépe porozumět tomu, proč byly technické kontroly vždy správnou odpovědí, nikoli masové zavádění přístrojů na ochranu dýchacích cest.
Respirační emise z „nemocných“ pacientů – PCR-pozitivní versus negativní výsledky testu:
Při výzkumu výdeje aerosolu u zdravých jedinců oproti SARS-CoV-2 PCR-pozitivním testovaným subjektům bylo více než 90 % procent emitovaných částic u PCR-pozitivních testovaných subjektů pod 0.3 µm a počty emitovaných látek byly provedeny srovnáním jedinců s různou závažností onemocnění s PCR-negativními subjekty.
"Medián vydechl počet částic byl vysoce významně zvýšený u pacientů pozitivních na SARS-CoV-2 PCR (1490.5/l [46.0–34,772.0 252.0/l]) ve srovnání se zdravými kontrolami (0.0/l [882.0–0.0001/l]; p < XNUMX."
Pokud použijeme rychlost dýchacích emisí 4.3-29 litrů za minutu (z EPA Exposure Factors Handbook), nejvyšší výstupní PCR-pozitivní rozsah 34,772 29 částic na litr vynásobený 1,008,388 litry za minutu je až XNUMX XNUMX XNUMX částic emitovaných za minutu. .
I když netvrdím, že všechny tyto částice byly jednotlivé virové částice nebo životaschopné virové částice, přesto existuje velmi významný rozdíl v látce emitované PCR-pozitivními a negativními jedinci (střední hodnoty 1,490.5 252 vs XNUMX). Poměr pro konverzi částic na PFU bude představen poté, co bude diskutována role PFU.
Velikosti částic a emise:
Studie již dříve probírala rozsahy měření velikosti emitovaných částic u pacientů s pozitivním a negativním SARS-CoV-2.
"Ohledně částice distribuce velikosti byly dostupné velikostní kanály (celkem 14 velikostních kanálů od 0.15 do 5.0 μm) analyzovány ve třech velikostních pásmech: <0.3 μm, 0.3–0.5 μm a >0.5–5.0 μm. U obou skupin byla většina aerosolů (>90 % ve skupině pozitivní na SARS-CoV-2 PCR a >78 % ve skupině -negativní) nalezena v nejmenším rozsahu (<0.3 μm). Zejména u COVID-pozitivní skupiny dominovaly nárůsty celkové koncentrace aerosolu nárůsty částic ≤0.3 μm.“
Deset jedinců z 64 hospitalizovaných pacientů, kteří byli zařazeni do vzorku, kteří patřili k nejzávažnějším případům, bylo odpovědných za přibližně 64.8 % procent počtu vydechovaných částic, takže je v tomto případě důležité podívat se na nejméně konzervativní rozsah výkonu a potenciál infekčnosti při výpočtu výkonu a minimální infekční dávky. Konkrétně v novinách bylo uvedeno:
"V případě SARS-CoV-2 PCR-pozitivní skupina, 15.6 % (n = 10/64) vykazovalo vysoké počty a byly zodpovědné za 64.8 % všech vydechovaných částic ve skupině. Navíc 15.6 %, což odpovídá 3.5 % všech pacientů (n = 10/288), bylo odpovědných za 51.2 % všech vydechovaných částic.
Pokud porovnáme ty, kteří trpí nejzávažnějším onemocněním, s mírou infekčnosti, můžeme porozumět více o produkci životaschopných částic u přenosných jedinců. Vzhledem k nízké produkci jak emitovaných látek, tak virionů u PCR-negativních a zotavujících se PCR-pozitivních testovaných subjektů, může být bezpečné spekulovat, že hovoří o nízké pravděpodobnosti asymptomatického přenosu, který je hlavním faktorem šíření viru.
Přítomnost kopií RNA versus koncentrace životaschopných virionů
Ne všechny kopie RNA nebo virové částice jsou schopny tvořit PFU, což vede k replikaci viru. I když byly poskytnuty údaje o tom, kolik infekčních jednotek je vytvořeno, je tomu tak ne rychlost produkce emisí. Toto jsou odhady celkové virové produkce během infekce.
"Dělení podle odhadů pro inverzní rychlost virové clearance dává odhadovanou celkovou produkci 3 x 109 do 3 × 1012 viriony nebo 3 × 105 do 3 × 108 infekční jednotky v průběhu charakteristické infekce."
Zjednodušeně, to je celková produkce 3 miliard až 3 bilionů virových částic nebo 300,000 300 až XNUMX milionů infekčních jednotek generovaných v průběhu nemoci.
Výstup virionu
Existují různé metody stanovení výstupu virionů, které nabízejí mírně odlišné rozsahy při pohledu vedle sebe. Některé studie ukazují celkový počet emitovaných virionů, například následující:
"Někteří pacienti mají virové titry, které přesahují průměrný titr Wölfela et al o více než dva řády, čímž se počet virionů v emitovaných kapičkách zvyšuje na více než 100,000 XNUMX za minutu mluvení.
Jiné studie uvádějí celkový počet částic a spoléhají na použití konverzních faktorů z celkového výstupu na životaschopné viriony. Důležité je zjistit, že celkový výstup virových částic se nerovná celkovým životaschopným virionům, což znamená viriony schopné vytvářet jednotky tvořící plaky (PFU).
PFU – Pochopení virových částic potřebných k vytvoření jednotlivých jednotek tvořících plak (PFU):
Zatímco všechny emitované virové RNA a virové částice nejsou schopné virové replikace a tvorby PFU, rozumí se, že každý PFU je tvořen jednou životaschopnou virovou částicí. Následující úryvky pojednávají o dopadu PFU na virové infekce a nástup.
"Test je navržen takže každý plak je výsledkem infekce zmnožením jediné infekční virové částice. Jako takové je PFU/ml považováno za míru počtu infekčních jednotek na mililitr (IU/ml), s výhradou, že si nelze být jistý poměrem plaků k infekčním částicím v aplikovaném alikvotu jedna ku jedné. “
"Pro většinu zvířecích virůk zahájení infekce stačí jedna infekční částice.
"Lineární povaha křivky dávka-odpověď ukazuje, že jeden virion je schopen iniciovat infekci. Vysoký poměr částic k pfu u mnoha virů však ukazuje, že ne všechny viriony jsou úspěšné. Vysoký poměr částic k pfu je někdy způsoben přítomností neinfekčních částic s genomy, které obsahují smrtelné mutace nebo které byly poškozeny během růstu nebo čištění.
"Obecně se předpokládá že plak je výsledkem infekce buňky jediným virionem. Pokud je tomu tak, pak by veškerý virus produkovaný virem v plaku měl být klon, jinými slovy by měl být geneticky identický.“

Abychom to shrnuli, jedna životaschopná virová částice nebo virion je schopna vytvořit jednu PFU, ve které se tato virová částice replikuje. Část vytvořené hmoty je výhradně virová RNA neschopná samostatně způsobit infekci a část vytvořené hmoty je schopná replikace a infekce.
Vztah mezi celkový výstup částic a tvorba PFU se nazývá poměr částic k PFU. U SARS-CoV-2 je poměr emitovaných částic k PFU 1000 1,000,000 až XNUMX XNUMX XNUMX.
Studie PFU a minimální infekční dávky
Naše dechová frekvence se liší v závislosti na věku a úrovni aktivity. Průměrná lidská dechová frekvence je 16-20 dechů za minutu. Pro účely této diskuse bude použita rychlost dýchání 4.3-29 litrů za minutu (z příručky EPA Exposure Factors Handbook). Tato reference udává rozsah až 53 litrů za minutu. Podíváme se na výstup jako viriony za minutu a minimální infekční dávku jako PFU a viriony pro přenos, protože oba jsou zkoumány v dostupném výzkumu.
Údaje o minimální infekční dávce (MID) z literatury:
Srovnávací studie různých respiračních virů a studie na zvířatech SARS-CoV-2 byly použity k přispění k mnoha odhadům MID, ale tento článek se v maximální možné míře zaměřuje pouze na lidské studie.
"Přestože MID SARS-CoV-2 u lidí potřebuje další výzkum, očekává se, že to bude přibližně 100 virových částic. Jediná studie na lidech týkající se koronaviru byla hlášena pro HCoV-229E a jeho MID je 9 PFU. Navíc, pokud je dominantním způsobem přenos aerosolu, pak by MID byla nižší.
"Vlastně, infekce na bázi aerosolu vyžadují menší dávky, např. ~100krát méně než kapénkové infekce.“
"Minimální infekční dávka míra SARS-CoV-2 způsobující COVID-19 u lidí v hodnocených průřezových studiích a studiích série případů byla nízká; ve studii série případů, která zkoumala infekční dávku u 273 vzorků od 15 pacientů pozitivních na SARS-CoV-2, byla zjištěná minimální infekční dávka 1.26 PFU in vitro v testu COVID-19-RdRp/Hel.1 V jiné studii 248 byly posouzeny oro-nosofaryngeální vzorky jedinců COVID-19 a infekční dávka byla hlášena jako 364 PFU.
"V případové studii která hodnotila 97 dětí ve věku 10 let a méně, 78 dětí ve věku 11–17 let a 130 dospělých, byla infekční dávka u dětí ve věku 11–17 let nižší než u dvou dalších skupin (125 PFU). Děti měly nižší růst živého viru, vyšší prahové hodnoty cyklu a nižší koncentraci viru ve srovnání s dospělými, takže děti nejsou hlavními přenašeči infekce. Děti ve věku ⩽10 let byly častěji asymptomatické než ostatní.
"Jeden z nejvíce dobře diskutovanou (sic) je studie provedená Basu et al., jejímž hlavním cílem bylo vyhodnotit velikost kapiček, které mají vysokou pravděpodobnost, že způsobí infekci. Ale kromě tohoto zjištění měli také některé body související s virovou zátěží, která může způsobit infekci. Zjistili, že počet virionů umístěných v těsně umístěném nosohltanu jedince během 2.5 hodiny se blíží (11/5) virionů za minutu × 60 min × 2.5 h = 330.
Srovnávací studie zahrnující jiné koronaviry ukázaly, že PFU mohou být u respiračních virů poměrně nízké.
"Odhadovaná infekčnost SARS-CoV-1 byl srovnatelný s jinými koronaviry včetně HCoV-229E, původce mírného nachlazení u lidí. ID10 a ID50 SARS-CoV-1 byly v experimentální studii hlášeny jako 43 a 280 PFU (400 TCID50).
"Lidské ID50 u sezónního koronaviru podtypu 229E, který způsobuje mírné běžné nachlazení u lidí, bylo hlášeno 13 TCID50. "
Hodnoty diskutované v poskytnutých studiích o SARS-CoV-2 byly 1.26, 100, 125, 330 a 363 PFU pro přenos, což opět hovoří o širokém spektru citlivosti.
Výstup životaschopných virionů versus potenciál prahu minimální infekční dávky
Použitím těchto dostupných čísel se můžeme vypořádat s tvrzením, že N95 poskytují smysluplnou ochrannou hodnotu před infekčními aerosoly, když se podíváme na výstupní příspěvky, potenciál infekčnosti emitované virové hmoty, rozsahy PFU, pak můžeme tyto rozsahy porovnat s hypotetickou perfektní záchytnou kapacitou N95. zachycující 95 % procent hmoty oproti zbývajícím nezachyceným 5 % procent. Znovu si všimněte, že N95 nejsou navrženy ani schváleny k zachycení <0.3 µm a diskutujeme o patogenu, který má minimální životaschopnou velikost částic 0.06-0.14 µm.
Respirační emise od přenosného jedince bylo prokázáno, že dosáhnou více než 100,000 750,000 virionů za jednu minutu, i když ne všechny emitované viriony lze považovat za infekční. Další výzkumné práce tvrdily, že výstup dosahuje až XNUMX XNUMX virionů za minutu (ale data podporující taková tvrzení chybí). Je třeba také poznamenat, že samozřejmě nevdechujeme všechnu hmotu jednotlivce, která vypršela, ale naše blízkost k přenosnému jedinci, rychlost jejich výstupu, trvání v prostoru a ventilace v daném prostoru jsou všechny faktory, které budou mít dopad na pravděpodobnost přenosu, který nelze vyjádřit lineárním nebo předvídatelným způsobem.
Ve studii jak jsme prozkoumali výše, nejvyšší výstupní PCR-pozitivní rozsah byl 34,772 64 částic na litr, přičemž ty, které emitovaly nejvyšší rozsahy výstupu, tvořily XNUMX % procent celkové emitované hmoty.
Nejprve vytvoříme hodinový výkon každého z těchto rozsahů, poté použijte poměr částic k PFU pro každý rozsah 1,000 1,000,000 až XNUMX XNUMX XNUMX.
Výstupní rozsah A
Hodina přenosného jedince v uzavřeném prostoru emitujícího 100,000 6 virionů za minutu by byla výstupem 100,000 milionů virionů (60 8×48 minut). Doba 100,000 hodin v uzavřeném prostoru se rovná 480 milionům emitovaných virionů (1,000 1,000,000 × 6,000 minut). S poměrem částic k PFU 48,000 8 až XNUMX XNUMX XNUMX nám to dává XNUMX XNUMX životaschopných virionů za jednu hodinu, XNUMX XNUMX za XNUMX hodin.
Hodnoty PFU z uvedených diskutovaných studií byly 1.26, 100, 125, 330 a 363 PFU požadované jako minimální infekční dávka. Vydělil jsem každé množství životaschopných virionů každou hodnotou PFU, abych dostal každý potenciál pro prahovou hodnotu MID.
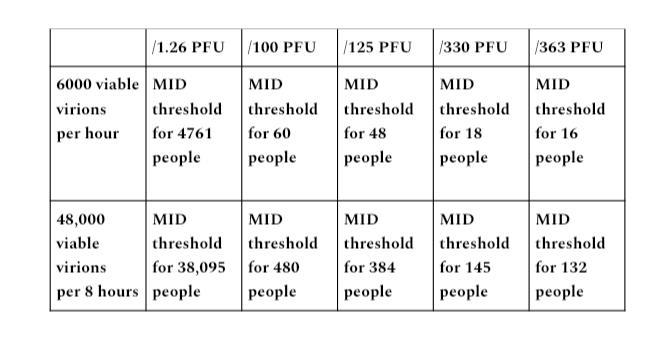
Výstupní rozsah B
Ve studii shromažďování pozitivních částic PCR bylo nejvyšším rozsahem shromážděných 34,772 64 částic na litr, přičemž ~ 10 % z celkového počtu emitovaných a spočítaných částic pocházelo z 2 zdrojů, které patřily k nejvíce nepříznivě postiženým infekcí SARS-CoV-34,772. . Pokud se podíváme na 29 1,008,388 částic vynásobených emisním objemem XNUMX litrů za minutu, výstupní rozsah je až XNUMX XNUMX XNUMX částic emitovaných za minutu.
EPA Exposure Handbook uvádí rozsah za minutu až 53 litrů za minutu, takže použití hodnoty 29 litrů za minutu není nejvyšší možný rozsah výkonu. Použijí se výstupní rozsahy 7 a 29 litrů za minutu, protože se jedná o rozsahy výkonu spadající do rozsahů úrovní sedavé až střední aktivity.
Při 29 litrech za minutu, násobeno 34,772 1,008,388 částicemi na litr (60 60,503,280 1,008,388 částic), při 60minutovém trvání výstupu je produkt 484,026,240 8 1,008,388 (480 XNUMX XNUMX × XNUMX) částic za hodinu a XNUMX XNUMX XNUMX za XNUMX XNUMX × XNUMX hodin minut).
S poměrem částic k PFU 1,000 1,000,000 až 60,503 484,026 8 pro COVID nám to dává XNUMX XNUMX životaschopných virionů emitovaných za hodinu a XNUMX XNUMX životaschopných virionů za XNUMX hodin.
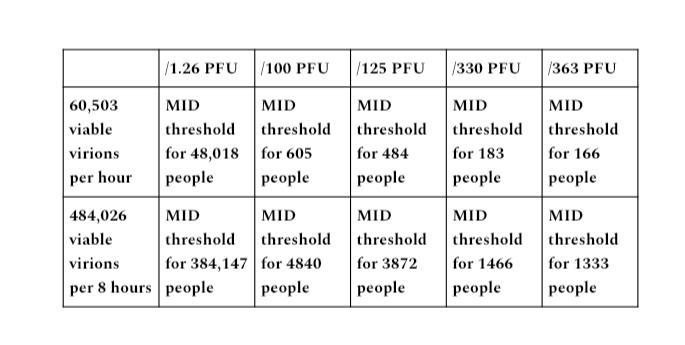
Tyto výpočty nám dávají výstupní potenciál přenosného jedince, pokud jde nejen o to, kolik virových částic je emitováno, ale také o potenciál pro dosažení prahu MID pro infikování daného počtu lidí, na základě které se používá hodnota PFU.
Zatímco rozsah PFU prokázaný pro SARS-CoV-2 je poměrně široký, měli bychom předvídat spektrum přenosnosti založené na individuálním zdravotním stavu a imunitní odpovědi. Zatímco 1.26 PFU se zdá být poměrně nízké, PFU pro SARS-Cov-1 se ukázalo být tak nízké jako 13 PFU, aby splnilo prahovou hodnotu MID pro nástup infekce.
I když se použije nižší emisní výkon 7 litrů za minutu, dává to rychlost 243,404 34,772 částic za minutu (7 14,694,240 x 234,404)), 60 116,833,920 243,404 částic za hodinu (480 8 x 1,000) a 1,000,000 1 14,604 (116,833 8 x XNUMX) částic. - hodinová perioda. Při aplikovaném poměru částic k PFU XNUMX XNUMX až XNUMX XNUMX XNUMX představuje jednohodinová perioda výstup XNUMX XNUMX životaschopných virionů a XNUMX XNUMX za XNUMXhodinovou periodu.

S těmito výstupními rozsahy sedavé až střední intenzity je mnohonásobně splněn práh MID pro všechny stanovené hodnoty PFU.
Proč N95 selhaly / selhávají / selžou
Respirátory s hodnocením N95 jsou navrženy a schváleny tak, aby zachytily 95 % neolejových látek větších než 0.3 µm. SARS-CoV-2 má minimální životaschopnou velikost částic 0.06-0.14 µm, což je hluboko pod prahovou hodnotou 0.3 µm, i když je vázáno na větší hmotu, takže se jedná o hypotetický předpoklad dokonalé záchytné kapacity pro takový rozsah částic, že tyto přístroje nejsou navrženy nebo schváleny k zachycení, ani jejich aplikační data neukázala jejich výkon na nebo blízko 95 % procent.
Pro účely cvičení v hypotetické dokonalé kapacitě zachycení jim poskytneme předpoklad dokonalé 95% míry zachycení. Pokud použijeme 5 % hodnot MID demonstrovaných v prokázaných výstupních rozsazích A a B, bude demonstrovat infekčnost životaschopných virionů oproti 5 % procentům, které nebyly nikdy zachyceny (např. žádný únik), pokud je hypotetická 95 % dokonalá míra zachycení je splněno.
Výstupní rozsah A
Výstupní rozsah B
29 litrů za minutu
7 litrů za minutu
Pokud předpokládáme hypotetickou dokonalou záchytnou kapacitu pro N95 s rozsahy velikostí částic hmoty, pro které tyto přístroje nejsou navrženy nebo schváleny, a použijeme zbývajících 5 % nikdy nezachycených, velká většina rozsahů výstupu versus PFU požadovaných ke splnění MID prahová hodnota stále umožňuje expozici mnohonásobku prahové hodnoty MID pro potenciální infekci mnoha jedinců v 1hodinových a 8hodinových periodách pro každý stanovený rozsah výstupu.
Shrnutí
Během vypuknutí SARS-CoV-2 jsme se stali laxní vůči našim zmírňovacím standardům, protože tento patogen není pro drtivou většinu lidí fatální, přičemž míra přežití se ukazuje kolem 99.8 % procent. Tato obratnost vůči reakci specifické pro nebezpečí je neuvěřitelně nebezpečná při aplikaci na smrtelnější patogeny a expoziční prvky.
Zkoumáním hypotetického nejlepšího scénáře můžeme lépe předpovědět, zda dané opatření bude mít zmírňující dopad na identifikované nebezpečí. Pro N95 versus výkon, poměr částic k PFU a MID pro SARS-CoV-2 nejlepší scénář hypotetického dokonalého zachycení hmoty, pro kterou tyto přístroje nejsou ani navrženy, ani schváleny, ukazuje, že jsou stále nezmírňující. toto nebezpečí a doporučení pro jejich použití by měla být okamžitě přehodnocena.
Dodatečné zdroje:
Pojednává o průměrné virové zátěži ze vzorků: https://www.nature.com/articles/s41586-020-2196-x.
Minimální infekční dávka
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC7090536/ (obecně pro MID, nikoli pro SARS-CoV-2).
Glosář
aerosol - částice rozptýlené ve vzduchu nebo plynu, definované jako menší než 5 mikronů.
asymptomatické (rozšířené) – teoretický koncept přenosu patogenu na jiné, aniž by se projevovaly žádné zavedené symptomy uvedeného patogenu.
nasycení atmosféry - množství životaschopné hmoty, která zůstává nahoře v uzavřeném prostoru.
emise – vydechované dýchací hmoty.
režim laminárního proudění – částice tekutiny sledující hladké dráhy ve vrstvách.
minimální infekční dávka – minimální množství nebezpečí, kterému musí být člověk vystaven, aby bylo možné předvídat nástup nemoci.
N95 - filtrační respirátor nezachycující částice, který dokáže zablokovat až 95 % hmoty nad 0.3 µm.
začátek – počátek onemocnění, které se ujme, jakmile je dosažena minimální prahová hodnota infekční dávky.
výstup - emise vypouštěné do daného prostředí přenosným jedincem.
výstup jako konstanta – jedinec v uzavřeném prostoru vypouštějící do dané atmosféry respirační aerosoly s infekčními částicemi, které s každým nádechem danou atmosféru více nasycují infekčními látkami.
poměr částic k PFU – poměr pro výpočty patogenního výstupu, který váží celkový počet emitovaných částic oproti částicím, které jsou životaschopně infekční.
PCR-negativní – daný testovaný subjekt nezíská pozitivní výsledek testu, když je testován metodikou PCR na daný patogen. PCR znamená použití techniky polymerázové řetězové reakce.
PCR pozitivní – daný testovaný subjekt obdrží pozitivní test při testování pomocí techniky polymerázové řetězové reakce na daný patogen.
perfektní snímací kapacita – zachycení nebezpečných látek se shodnou procentuální účinností danou produktem jako jeho hypoteticky nejlepší možná míra.
Plaque Forming Units (PFU) – vytvoření PFU vyžaduje, aby jeden virion infikoval hostitelskou buňku, kde začíná virová replikace. Pro nástup onemocnění je vyžadován práh daného počtu PFU, známý jako minimální infekční dávka.
kopie RNA - genetický materiál potřebný k vytvoření kopií proteinů v buňce. Kopie RNA se nerovnají životaschopným virionům schopným replikace.
TCID50 – zkratka pro infekční dávku pro tkáňové kultury, což je ředění viru potřebné k infekci 50 % buněk v kultivačním testu.
virová nálož - množství virových částic v dané látce, emisi nebo v těle přenosného jedince.
virová životaschopnost - viriony schopné infikovat buňku a vytvářet jednotky tvořící plaky (PFU).
virion nebo životaschopný virion- kompletní infekční virová částice.
Publikováno pod a Mezinárodní licence Creative Commons Attribution 4.0
Pro dotisky nastavte kanonický odkaz zpět na originál Brownstone Institute Článek a autor.









