
Během posledních desetiletí své kariéry jsem strávil nespočet hodin prací na ochraně Američanů výzkumem bezpečnosti drog. Moje vzdělání a kariéra mě zavedly přes asi půl tuctu univerzit, Big Pharma a na FDA pod třemi prezidentskými administrativami. Bezpečnost léčiv zvažuje, proč jeden jedinec může užívat farmaceutický produkt a nemá žádné nežádoucí účinky, zatímco jiný jedinec by mohl užívat stejný produkt, ale mít nežádoucí účinky až do trvalé invalidity nebo smrti včetně. Studium bezpečnosti léků standardně bere v úvahu také neklinické aspekty výroby a kvality léků.
Vzhledem k tomu, že kvalita léků je základním faktorem při posuzování bezpečnosti léků, moje cesta k ochraně Američanů vedla k mé koncepci a založení první světové „analytická lékárna"Posláním vědeckého ověřování farmaceutických produktů z míst, jako je Indie a Čína, před jejich vydáváním pacientům. Bohužel snaha o velkorysost nad etikou a ochranou pacientů vedla k tomu, že finanční management této společnosti rozsáhlý Porušení FDA a obvinění soudci z výroby nepravdivá vědecká tvrzení (to vše se shodou okolností stalo po mém odchodu).
Bez vnějšího potvrzení kvality léku jsou Američané zcela závislí na FDA a výrobcích, aby posoudili a potvrdili čistotu produktu. Bezpečnost léků se ukázala jako významný problém, pokud jde o injekce mRNA Covid. Bohužel, pokud by někdo chtěl provést vlastní analýzu injekcí mRNA, udělal to nemají náležitě podrobný seznam složek, se kterými by bylo možné je porovnat, nebo dokonce přístup k zavedené regulační metodice, jak správně testovat čistotu.
Je to kvůli výrobcům a FDA zvažuje všechny složky těchto injekcí mRNA, včetně sekvence mRNA plus vlastností lipidových nanočástic (LNP), včetně poločasu rozpadu, struktur LNP, povrchových modifikací, počtu/typů LNP na dávku a bodů připojení na řetězec mRNA, blíže nespecifikovaný nebo „obchodní tajemství“.
Kromě toho FDA navíc zvažuje metodiky o tom, jak testovat čistotu injekcí mRNA, je také obchodním tajemstvím.
Podpora obou stran a stovky miliard dolarů daňových poplatníků, ale BEZ transparentnosti?
Utajení mRNA Covid existuje, přestože administrativa Trumpa i Bidena navrhla plnou transparentnost injekcí mRNA až do bodu zrušení práv duševního vlastnictví Covid mRNA. Navzdory tomu FDA i výrobci povolují/udržují pevné patenty, včetně základních údajů o těchto střelách, jako obchodní tajemství. Činí tak navzdory tomu, že všichni výrobci vakcíny Covid obdrželi stovky milionů dolarů daňových poplatníků podle Forbes/Statista publikace.
Studium epidemiologie bezpečnosti léků je dost obtížné. Bez ověřitelné čistoty/konzistence produktu je úplné hodnocení bezpečnosti nemožné.
Úplná transparentnost všech složek a opatření na kontrolu kvality jsou důležité nejen proto, že byly těžce financovány daňovými poplatníky ve stovkách milionů dolarů, ale také proto, že se objevila spousta otázek o bezpečnosti a účinnosti injekcí mRNA Covid.
Kromě toho, že byly mimořádně složité, jejich schválení regulátoři urychlili poté méně než jeden rok. Většina léků a vakcín obvykle zabírá deset let plně otestovat bezpečnost/účinnost a zkontrolovat a schválit. Kromě toho, že složky jsou zcela nové, velmi složité a první svého druhu podávané v masivním měřítku, vývoj zahrnuje dlouhodobé hodnocení klinické bezpečnosti/toxicity a epidemiologické přehledy byly urychleny a pravděpodobně nebyly před propuštěním zcela objasněny.
Ověřování ingrediencí FDA, transparentnost a „pravdivost“ mají precedenty pocházející z 1800. století:
Analytické ověření a transparentnost složek nebo „pravda v označení“, kde je obsah lahve požadováno aby odpovídaly uvedeným ingrediencím před založením FDA, zpět do roku 1862. Dnešní FDA se ve skutečnosti zrodilo z toho, co začalo jako jediný zaměstnanec „Department of Chemistry“ zaměstnaný na ministerstvu zemědělství USA.
Falšování, (změněné nebo toxické přísady) nesprávné označení (obsahuje nepravdivé označení nebo je jinak zavádějící nebo obsahuje nesprávná lékařská tvrzení), popř nesprávné označení (obsahuje přísady, které nejsou uvedeny na etiketě produktu) mají v Americe dlouhou, ošklivou historii. Předpokládalo se, že křiklavost dosáhla vrcholu na počátku až v polovině 19. století – nebo alespoň tehdy se stala identifikovatelnou – protože teprve v roce 1862 byly vyvinuty technické procesy k analýze a odhalování podvodů s přísadami. Předtím takzvaní „cestovní medicinmani“ nazývající se „lékaři“ (vždy s pochybnými nebo neexistujícími doklady) prodávali lahve s „léčivými“ produkty, jejichž etikety obsahovaly pouze mlhavý nebo neškodný obsah, jako je např. “vitamíny""bylinné extrakty,", nebo "hadí olej“ – nebo často nemají vůbec žádný seznam složek.
Tehdy mnoho zbožných, puritánských obyvatel Nové Anglie, kteří z náboženských důvodů ano nikdy dotknout se alkoholu, kupoval by tyto roztoky od těchto prodavačů a byl by nevědomky podveden ke konzumaci roztoků, které neobsahovaly pouze alkohol, ale také narkotika jako opium a/nebo kokain. Pod záminkou zlepšení nesmyslně širokého hojnosti nemocí se u pacientů místo toho vyvinula trestající závislost a/nebo bylo jejich zdraví negativně ovlivněno těmito ranými „drogovými dealery“.
Jak problém narůstal, federální vláda si toho začala všímat. Nakonec, Zákon o čistých potravinách a léčivech byl schválen v roce 1906 a vedl k vytvoření Food and Drug Administration (FDA).
[FDA měl a formativní povinnost zajistit, aby léky nesly pravdivá označení a splňovaly určité normy pro čistotu a sílu.
Pamatujte si, že téměř 120-letý pravdivý požadavek na označování a část „čistota“ zákona o čistých potravinách a léčivech z roku 1906, když jste četli o ověřovacím testování mRNA a průhlednosti přísad.]
Jaké „pravdivé“ a „čisté“ ověřovací testování přísad probíhá u produktů regulovaných FDA?
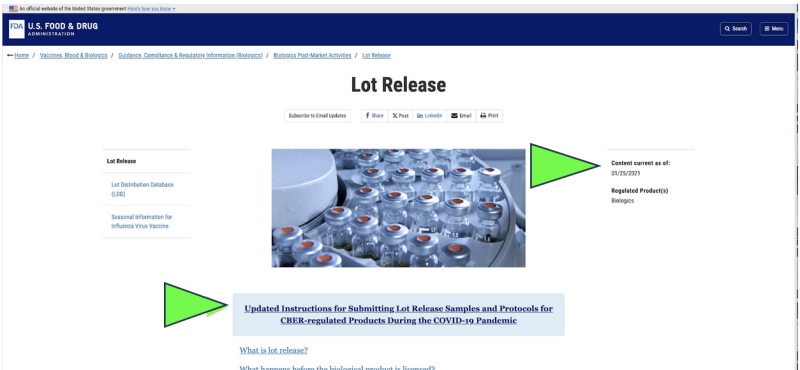
V roce 2021 se FDA rozhodl začít sledovat americkou farmaceutickou kvalitu prostřednictvím a vzdálený sběr of zaslání vzorků poštou pro drogy jako náhradu za živé kontroly zařízení kvůli pandemii Covid. Bylo to legální? Mohlo by to být někdy považováno za vědecky vhodné? Dnes, navzdory tomu, že pandemie skončila, v současnosti probíhá jediné oficiální testování uvolňování léčiv žádný Covid mRNA farmaceutický přípravek objeví se na ještě provede FDA prostřednictvím výrobce dodaného, “zasláno poštou“ vzorek podle a snímek obrazovky aktuálního webu FDA. Je zřejmé, že metoda odběru vzorků „poštou“ je daleko odlišná a potenciálně méně spolehlivá než přímý odběr vzorků metodou přímého osobního odběru. Navzdory tomu FDA tvrdí, že má „nejvyšší standard na celém světě pro odběr vzorků a testování. "
Kromě toho FDA navrhuje další pokrok ve své politice vzdáleného testování „zaslaného poštou“ s a nově navrhovaný dokument s pokyny.
Ačkoli existuje pouze jako „návrh“ dokumentu FDA, oficiální webové stránky FDA to ukazují Zdá se, že zasílání vzorků poštou již bylo implementováno minimálně od ledna 2021. Zdá se, že FDA prosazuje výsledky těchto testů zaslaných poštou jako jejich nezávislé ověření.
Kromě toho dole na první stránce návrhu FDA dokument navrhuje rozšíření „vzdáleného testování“. Aktuálně uvádí každý divize FDA pro regulaci produktů ve FDA, což znamená, že jde o návrh politiky pro celou agenturu.
Kompletní seznam obsahuje:
- Úřad pro regulační záležitosti
- Úřad pro potravinovou politiku a reakci
- Kancelář kombinovaných produktů
- Centrum pro biologické hodnocení a výzkum
- Centrum pro hodnocení a výzkum léčiv
- Centrum pro přístroje a radiologické zdraví
- Centrum pro bezpečnost potravin a aplikovanou výživu
- Centrum pro tabákové výrobky
- Centrum veterinárního lékařství
Je odběr vzorků kontroly kvality „zaslaný poštou“ FDA vhodný? Co když inspekce restaurací ministerstva zdravotnictví státu odráží politiku FDA?
Tato metodika odběru vzorků „mail-in“ je podobně absurdní, jako když například státní ministerstvo zdravotnictví monitoruje restaurace tím, že je žádá, aby pravidelně „posílaly“ různé položky ze svého jídelníčku do testovacího zařízení, aby zdravotní oddělení mohla testovat potenciální potraviny. -rozená kontaminace a/nebo žádat restaurace, aby slíbily, že otestují položky menu samy. Co kdyby ta restaurace byla v Číně? Co kdyby ta restaurace byla v Indii? Nebo jakákoliv jiná země známá tím, že má propastná historie podvodů a kontroly kvality problémy?
Tato metodika by byla nepřijatelná pro restaurace i farmaceutické společnosti, a to z důvodů, které jsou zřejmé: výrobci by mohli zasílat vzorky, které preferují – ne nutně reprezentativní vzorky šarže. Zjevně to není totéž, jako když inspektoři FDA získávají vzorky během neohlášených kontrol celého zařízení.
Podle analogie s restaurací by samozřejmě všechny restaurace předložit vzorky třídy „A“. což by nemuselo být nutně reprezentativní pro to, co spotřebitelé dostávají.

Kontrola kvality: Co je to farmaceutické „testování uvolňování“ a proč je důležité?
Dnes FDA dohlíží na kvalitu a obsah $2.7 bilion hodnotu produktu ročně, ale zdá se, že potlačuje kritická hodnocení a výsledky ověřování přísad. FDA má chránit Američany dirigováním obsáhlý analytické testování jako kontrolní součet pro zajištění přesnosti přísad. Výsledky by měly být transparentní pro daňové poplatníky, kteří je financují FDA 6.6 miliardy dolarů rozpočet. Toto vědecké ověření se označuje jako farmaceutické „testování vydání.“ Testování uvolňování je technický termín označující proces zahrnující řadu používaných instrumentálních analýz komplexně testovat produkty na čistotu, koncentraci, konzistenci, identitu a nečistoty jakéhokoli druhu.
Celý FDA se zrodil z jednoho zaměstnance „Department of Chemistry“ z roku 1862 a potřeby transparentnosti a ověřování přísad. Dnes se tento zaměstnanec rozrostl do společnosti celé oddělení FDA 1,300 vědců a podpůrného personálu předpokládaně věnované ověřování přísad prostřednictvím testování uvolňování léčiv. FDA Úřad pro farmaceutickou kvalitu (OPQ) má zajistit, aby léčiva přesně odpovídala obsahům uvedených složek, bez kvalitativní/nečistotné (kvalitativní) nebo obsahové (kvalitativní) variability. Pravidla, která to vyžadují, jsou velmi konkrétní a podrobná 21 CFR § 201.10.
Jak FDA ověřuje injekce mRNA pro kontrolu kvality:
Výsledky kontroly kvality z testů z injekcí mRNA byly obzvláště důležité, protože jsou velké, složité a byly rychle vyrobeny. Zatímco daňoví poplatníci jsou při ověřování kvality injekce mRNA a sdílení výsledků závislí na FDA, FDA zdá se, povinni chránit přísady výrobců na úkor i té nejzákladnější transparentnosti, pokud jde o produkty mRNA Covid. I když se zdá, že FDA sbírá vzorky, jejich metodika „mail-in“ je zásadně chybná. Navíc FDA nesdílí výsledky těchto testů nikde, kde bych je mohl najít.
Jinými slovy: během pandemie, kdy byly na Američany „warpovou rychlostí“ vhazovány zcela nové, široce implementované výstřely mRNA a kdy se Amerika nejvíce spoléhala na kvalitativní/regulační povinnosti FDA, FDA akceptovala samoobslužné „poštou- in” testování a/nebo výsledky kontroly kvality. FDA to nezvážila Výrobci mRNA přiznali, že „bojují[d]“ reagovat na výrobu a „snaží se“ držet krok s výrobními procesy? Výrobci složek mRNA dále uvedli, že snahy vyhovět potřebám byly „bezprecedentní“.
Prohlášení, jako je toto, nezvyšují důvěru spotřebitelů v kvalitu a jsou ilustrativním příkladem obrovského upscalingu těchto komplexních produktů, které by měly zaručit zvláště ostražitý a osobní prohlídka zařízení a vyrobených produktů FDA, ať už pandemická nebo ne. Jeden výrobce složek mRNA například uvedl, že náhle zvýšili svou produkci 50 fold.
Uprostřed této nové technologie prosazované „warpovou rychlostí“ nepožadoval žádný z 1,300 vědců OPQ z FDA živé inspekce, nebo alespoň nenabízel, že udělá něco jiného, než žádá o potenciálně sporné „zaslané“ vzorky. na testování?
Zjevná otázka zní: proč FDA neodebíral vzorky přímo? I v případě pandemie mohl FDA kontrolovat zařízení v nebezpečných oblecích nebo – nebo na velmi nejméně – rozhodli se odebírat vzorky z lékáren, nemocnic nebo ve skladech distributorů.
Skrytá metodika pro testování složek injekce mRNA:
Kromě absence výsledků testování a pochybných výsledků odběru vzorků „zaslaných poštou“ – FDA ano navíc skrývá svou ověřenou metodologii a brání ostatním v provádění jejich vlastních nezávislých analýz kvality/čistoty injekcí mRNA.
Nezávislá analýza čistoty a potenciální kontaminace léků ve srovnání se seznamem složek je něco, o co jsem se sám pokoušel, když jsem koncipoval první na světě analytická lékárna. Nicméně, protože mRNA výstřely jsou novou technologií s méně než zcela transparentním seznamem složek, testovací metodologie, kterou by bylo nutné použít, není přímočará, jako by tomu bylo u jiných léků s malou molekulou. Každý, kdo se snaží vyhledat úložiště, stabilitu, specifičnost, chemii, citlivost nebo dokonce základní metodologii testování validace a/nebo výsledků, je zablokován zprávou FDA obsahující směšně invazivní redigování, takže i to nejzákladnější vědecké chápání toho, jak potenciálně hodnotit výsledky nebo provedení testování nemožné.
Jako působivý vizuální příklad je jedna redigovaná stránka v delším regulačním souhrnu FDA (zobrazeno níže) součástí 127stránkový dokument (z toho pouze 63 stran bylo sdíleno a z těchto 63 stran bylo asi 50 % zredigováno) o tom, jak hodnotit čistotu, koncentraci a další analytická měření injekcí mRNA.
Ti, Redakce FDA (b) (4). specifikované podrobné redakce používané k „chránit obchodní tajemství a důvěrné obchodní nebo finanční informace.“ Ale je opravdu vhodné označit to za „komerční“, pokud byl výzkum/vývoj/produkt financován stovky milionů dolarů daňových poplatníků?

Bez seznamu složek nebo testovací metodologie je nemožné, aby kdokoli jiný mimo FDA nebo výrobce přesně věděl, jak produkt zkontrolovat falšování (změněné nebo toxické složky) nebo nesprávné označení (protože úplný seznam složek včetně nukleotidové sekvence a konfigurace lipidových nanočástic jsou na etiketě výrobku zvláště vágní).
Absence metodologie je obzvláště problematická, protože nové předběžné údaje využívající nezávislou metodologii prokázaly Kontaminace DNA v injekcích mRNA Covid.
Pokud tedy někdo zvenčí tvrdil, že testoval a našel nečistotu v záběrech mRNA a požádal FDA nebo výrobce o odpověď, setkal by se s nějakou odpovědí, která by uváděla něco v tomto smyslu:
- Nepoužili jste ověřenou/vhodnou metodologii testování, abyste dospěli ke svým závěrům, a proto jsou vaše analýzy neplatné.
K tomu by se nezávislá laboratoř pokusila vyžádat si testovací metodologii z dokumentace schválené FDA (tj. úplný dokument obsahující Obrázek 5) dotazem: „Dobře, rád bych to otestoval pomocí vaší schválené metodiky; řekneš nám, co to je?"
- FDA nebo výrobce by odpověděli něco ve smyslu: „Co jsme ochotni prozradit o použité metodologii, která není důvěrná, lze nalézt online nebo prostřednictvím žádosti FDA FOIA“ …kde by se s nimi setkali následující silně redigovaný dokument, kde je vše vzdáleně smysluplné pokryto (b)(4) redakcemi.
Čtení mezi řádky: Je zřejmé, že jak výrobci, tak americký FDA nechtějí, aby kdokoli jiný než oni sami znali kompletní složky nebo dokonce testovali injekce mRNA na čistotu a konzistenci.
Podle úředníků FDA: Pharmaceutical Manufacturing je Vysoce Sklon k chybám:
Mnoho věci se mohou během farmaceutického výrobního procesu pokazit – a také se dějí. Kromě potenciálních nekonzistencí s injekcemi mRNA/LNP, kvalitativní a kvantitativní problémy implikují každý Farmaceutický výrobek regulovaný FDA. Dokonce i sněmovna a Senát formálně uznaly zprávy o selhání FDA zajistit americký farmaceutický dodavatelský řetězec. Většina americký lék spotřebitel-koncový uživatel produktuse vyrábí v zámoří v zemích jako Indie a Čínaa další země s nízkými náklady na pracovní sílu ne uznávaný pro vysokou úroveň kontroly kvality. Federální rejstřík je prošpikován zprávami o porušení v indických a čínských výrobních závodech.
Certifikuje FDA také tyto závody – včetně těch s dlouhou historií porušení – prostřednictvím systému „mail-in“ do FDA? Je neuvěřitelné, že odpověď na otázku je něco, co by každému, kdo se zabývá farmaceutickou kvalitou, velmi znepříjemnilo.
Zatímco a Six Sigma Úroveň přesnosti je již dlouho cílem pro kvalitu a bezpečnost v automobilovém průmyslu, počítačích, mobilních telefonech a dalších high-tech výrobě, zdá se, že byla většinou přehlížena, pokud jde o farmaceutickou výrobu.
Představitelé FDA zveřejnili údaje o odhadu 2-3σ (sigma) nepřesnosti ve farmaceutické výrobě. Kvalita 2σ odpovídá 308,537 1,000,000 defektů na XNUMX XNUMX XNUMX příležitostí. (Pravděpodobně existuje mnohem více než 1,000,000 XNUMX XNUMX příležitostí k chybám, pokud jde o farmaceutickou výrobu.) FDA si je toho vědoma na nejvyšších úrovních vedení; ve skutečnosti proud Šéf Úřadu pro farmaceutickou kvalitu FDA Michael Kopcha dokonce napsal a zveřejnil výše uvedený výpočet Six Sigma, bědující nad nepřesnou povahou farmaceutické výroby zpět 2017.
Šířka chyb pro produkty mRNA a/nebo jejich LNP by mohla být rovnoměrná méně přesnější než 2-3σ (čím nižší je σ, tím je produkt chybnější), protože obsahují nukleotidový materiál a nové LNP, což je činí podstatně složitějšími než léčiva s malou molekulou – bez ohledu na to, že jsou vyvíjeny, vyráběny a uvolňovány na „ Warp rychlost."
Dokonce i FDA a její úředníci uznávají neodmyslitelnou výrobní nepřesnost, proč v širém světě sportu neplní FDA své bezpečnostní poslání tím, že veřejně sdílí své testování uvolňování mRNA technologie s americkou veřejností, která je financuje?
Znovu před rokem 1862? Jsou injekce mRNA jedinými léky, na které Američané nemají Kompletní Informace o složkách?
Nejasnost ohledně počtu sekvencí záběrů mRNA a dalších kritických informací je v přímém kontrastu s jiným lékem na bázi RNA, který schválil FDA – patisiran (Onpattro®). Onpattro transparentně poskytuje sekvenci, molekulovou hmotnost a miligramovou sílu svých produktů v rámci oficiálního FDA označení balení jak je znázorněno na úryvku níže:


Nedostatek Covid mRNA Dávková specificita: 0.3 ml (nebo 0.5 ml) čeho?
V současné době stále nemáme základní informace o složkách jakékoli injekce mRNA Covid. Lékárníci vědí pouze uvést konkrétní objem tekutiny, a zdánlivě tak učinil bez otázek. Normálně by oficiální označení balení FDA mělo uvádět skutečné složky v tomto objemu, ale ne pro štítky Covid mRNA: jednoduše uvádějí 0.3 ml (nebo 0.5 ml) jako „dávkovou formu a sílu“.
Navíc, jak by vám mohl říci každý student střední školy, 0.3/0.5 ml je a objem, a pevnost. Neznáme žádná kvantitativní specifika toho, co je obsaženo v těch 0.3/0.5 ml, jako například: Kolik částic LNP? Jaká velikost/morfologie těchto LNP? Kolik sekvencí mRNA je v tomto objemu?




Je toto označení odpovídajícím způsobem transparentní nebo „pravdivé označení“ ze strany FDA?
Výše uvedený úryvek z příbalového letáku obsahuje všechny informace, které výrobci sdílejí se spotřebiteli ohledně dávky – která je žalostně nedostatečná ve srovnání se všemi ostatními etiketami FDA – nebo kohokoli, kdo by chtěl vědět něco jiného, než kolik tekutiny k injekci a koncentraci 30 nebo 100 mcg blíže nespecifikované sekvence mRNA.
Zdá se, že pozoruhodná nepřesnost tohoto štítku povolená FDA je v rozporu s jeho téměř 120 let starým štítkem: „vyžadující, aby potraviny a léky nesly pravdivá označení a splňovaly určité normy pro čistotu a sílu. "
Je to to, co vydává FDA jako „pravdivý“ seznam složek? (Vidět 21CFR § 352, a 21 CFR § 201.10 týkající se „prohlášení o složkách“ a „nevhodně označených léků a zařízení.“)
Otázka zní: má seznam neznámých nebo nespecifických složek, které nikdo kromě výrobce nemůže dešifrovat opravdu splňují duch nebo zákonné požadavky „označování? Je toto označení to, co americký FDA považuje za „pravdivé“? Na čí straně je vůbec FDA; výrobci nebo spotřebitelé?
Kromě toho, že to není přímo specifikováno, přesný počet řetězců LNP ani mRNA v injekci 30 nebo 100 mcg nelze ani extrapolovat. stechiometricky nebo na základě Avogadrovo číslo, protože sekvence mRNA, molekulová hmotnost a/nebo složka/konfigurace LNP nejsou nikde v oficiálním značení FDA uvedeny.
Jak může někdo vědět, zda je počet řetězců mRNA pro kódování spike proteinu pro Covid úměrný zátěži inokula Covid, které by člověk obdržel od komunitní infekce? Odpovědět: nemohou.
Jsou Covid mRNA injekce Přiměřeně označeno/chybně označeno?
21 CFR 211.125 specifikuje "Nad označením vydávaným pro použití při označování léčivých přípravků musí být vykonávána přísná kontrola,“ ale zdá se, že FDA byla tak laxní se svým schváleným značením injekcí Covid mRNA navzdory skutečnosti, že každý jiný lék – včetně Onpattro na bázi mRNA – tyto informace specifikuje. Historicky jsou regulační rozhodnutí FDA (např. které informace zahrnout do označení produktu) založena na prioritě a injekce mRNA Covid byly zjevnou odchylkou od historické a právní priority FDA. Tato pozoruhodná absence dat a nedostatek jasnosti se tak trochu vrací do dob Morleyova játra a ledviny Cordial koncem 1800. století. Rozdíl je v tom: tehdy FDA neexistoval, ale dnes existuje FDA s ~20,000 XNUMX zaměstnanci, z nichž alespoň někteří údajně věřili, že toto označení je transparentní a „pravdivé“.
Uvádění neznámé/nerozluštitelné/obskurní přísady, kterou nikdo nikdy nemohl přesně určit jako pravděpodobnou, není to, co zákonodárci zákona o čistých potravinách a léčivech z roku 1906 zamýšleli, když specifikovali pravidla FDA o „pravdivém označování“. Kromě toho: skutečnost, že dávky jsou zdvojnásobeny na objem od různých výrobců (30 mcg/0.3 ml vs 100 mcg/0.5 ml) znamená, že tyto sekvence mRNA se zdají být značně odlišné v délce nukleotidů a naopak by měly více a různých LNP plus přílohy. Znamená to, že sekvence mRNA použité k transkripci spike proteinu mají přibližně dvojnásobnou velikost (10 mcg/0.1 ml versus 20 mcg/0.1 ml) ve srovnání s různými výrobci, nebo k rozdílu v délce nukleotidů přispívá něco jiného?
Pro laika, který stále čte až sem (mimochodem chvála): Nedostatek podrobných informací na štítku by mohl být jako plošná reklama na dům na prodej s prohlášením, že je vyroben ze dřeva a cihel, na cementové desce – ale nezobrazuje se jakékoli obrázky domu (např. sekvence) a nesdílení jeho čtverečních záběrů (např. molekulové hmotnosti). V každém případě je nedostatek informací nedostatečný a odchylka od tradičních standardů.
Každý jiný lék schválený FDA – včetně jiných léků mRNA – obsahuje úplné informace o složkách svých produktů, včetně strukturní reprezentace a molekulová hmotnost jejich produktu, aby lidé přesně věděli, co dostávají.
Je to pravda: Hledejte jakoukoli drogu, na kterou si vzpomenete Databáze Drugs.com a všimněte si, jak všechny štítky poskytují strukturu a/nebo molekulovou hmotnost. Důkaz, že injekce mRNA Covid jsou a nápadný výjimka z historické schvalovací praxe FDA a pravidla „pravdivého označení“.
Podrobnosti dánské studie z roku 2023 Významná klinická variabilita mezi šaržemi injekcí mRNA Covid-19 mRNA:
Zdá se, že neexistence jakékoli transparentnosti, pokud jde o potenciálně neplatnou validaci testování „zaslaným poštou“, poskytla výrobcům další kriticky důležitou část toho, na co dohlíží FDA: potenciální klinické projevy na variacích šarží/šarží injekcí mRNA. Retrospektiva Dánská bezpečnostní studie publikované dříve v roce 2023 podrobně popsaly vysoce odchylný vzorec hlášení nežádoucích účinků z injekcí mRNA Pfizer-BioNTech BNT162b2 v korelaci s dánským systémem hlášení nežádoucích účinků DKMA.
V následujícím čárovém grafu představují různé barevné tečky různé šarže injekcí mRNA společnosti Pfizer-BioNTech. Rozdělil šarže do tří různých kategorií; vysoký – nízký – až (téměř) chybějící počet hlášených skupin nežádoucích účinků (modré, zelené a žluté grafy).
Jinými slovy: Zdá se, že zdánlivě „ekvivalentní“ produkty od stejného výrobce mají velmi rozdílný výskyt nežádoucích účinků podle šarže, přičemž každá z těchto šarží představuje stovky tisíc injekcí mRNA.
Když byly přidány odpovídající lineární regresní čáry, objevil se konkrétní vzor:
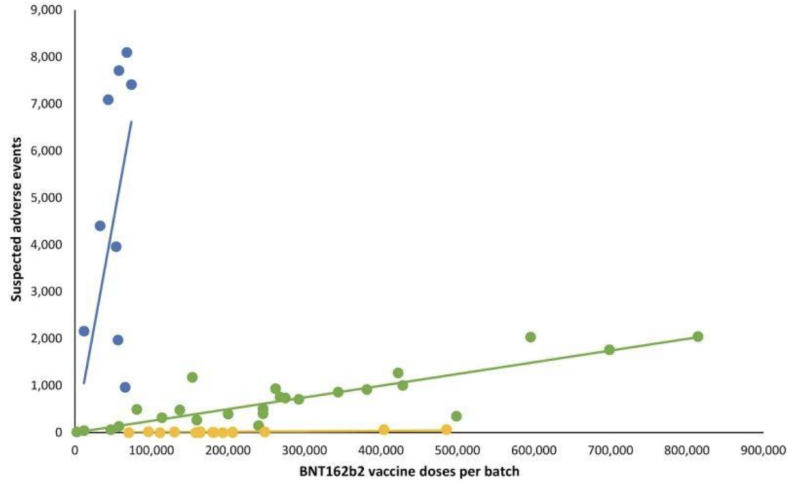
Mezi důležité otázky týkající se pozoruhodných rozdílů nežádoucích účinků mezi šaržemi mRNA Covid-19 patří:
- Mohou být odchylky nežádoucích účinků způsobeny kvalitativními nebo kvantitativními odchylkami v sekvencích mRNA nebo počtem řetězců mRNA mezi šaržemi?
- Mohou být odchylky nežádoucích účinků způsobeny kvalitativními nebo kvantitativními rozdíly ve velikosti/morfologii nebo množství LNP mezi šaržemi? Jaké testy byly provedeny zajistit bezpečnost různých LNP používané v injekcích mRNA?
- Byly ty šarže, které odpovídaly datovým bodům žlutá versus zelená versus modrá, nějak kvalitativně nebo kvantitativně odlišné?
- Vedlo povýrobní skladování/manipulace ve správním zařízení (nebo někde jinde v dodavatelském řetězci) k proměnlivosti produktu?
- Jaká je Sigma/chybovost tohoto a dalších produktů pocházejících z konkrétního výrobního závodu/vedoucího směny odpovědného za výrobu?
- Pocházely přísady z těchto produktů mRNA Covid z Indie nebo Číny oproti jiným, v závislosti na šarži?
- Jaké procento šarží produktů Covid mRNA bylo testováno prostřednictvím osobního odběru inspektorem FDA oproti tomu, které byly „zaslány“ od počátku do dnešního dne? Byla každá jednotlivá šarže testována pouze jednou z těchto dvou metod sběru?
- Provedl FDA ověření propouštění u šarží dánského systému hlášení nežádoucích účinků DKMA? Pokud ano, proč FDA nezveřejňuje tyto konkrétní výsledky testování? Pokud ne, proč nebylo testování provedeno?
- Existuje zásadní problém s konzistentní produkcí sekvencí LNP a/nebo mRNA spolehlivě a bez kontaminace?
Výsledky dánské studie a výše uvedené otázky o nežádoucích účincích by se mohly *začít* řešit, ale ne bez toho, aby FDA nezávisle sdílela výsledky svých zjištění z testování uvolňování. Jak to tak je, kvůli všudypřítomným redakcím FDA (b) (4) nikdo nezná ověřenou metodiku testování Covid mRNA záběrů or přesně které šarže v dánské studii byly nebo nebyly testovány or výsledky těchto dávkových testů.
…Takže znovu, i kdyby se FDA rozhodl zveřejnit tyto výsledky testů šarží, jak spotřebitelé vědí, zda jsou tyto výsledky reprezentativní pro uvedené šarže, protože výrobci si sami vybírají, které vzorky zašlou poštou?
Základním a základním požadavkem FDA je nezajištění transparentnosti složek a zajištění kvality pomocí vhodné metodologie odběru vzorků. Ve skutečnosti to byl hlavní důvod pro vytvoření FDA! Nezaslouží si Američané lepší transparentnost, dohled a zákony o „pravdivém označování“, pokud jde o naše léčiva – zvláště když tyto zákony byly přijaty před více než 100 lety?
Publikováno pod a Mezinárodní licence Creative Commons Attribution 4.0
Pro dotisky nastavte kanonický odkaz zpět na originál Brownstone Institute Článek a autor.









