Telegraph nedávno oznámila, že veřejnosti bylo řečeno, aby přestala užívat léky proti kašli a nachlazení kvůli obavám o bezpečnost týkající se drogy, folkodinu, opioidního léku na potlačení kašle.
Dvacet běžných léků proti kašli a nachlazení, včetně kapslí Day and Night Nurse, bylo naléhavě staženo z trhu na příkaz regulátorů léků kvůli obavám z „velmi vzácného“ rizika anafylaxe, život ohrožující nežádoucí příhody.
Oznámení „Class 2 Medicines Recall“ převzato z vlády Spojeného království webových stránkách , je zobrazen níže.

Pokud jde o mRNA vakcíny COVID-19, regulační dvojí standardy nebyly nikdy tak do očí bijící.
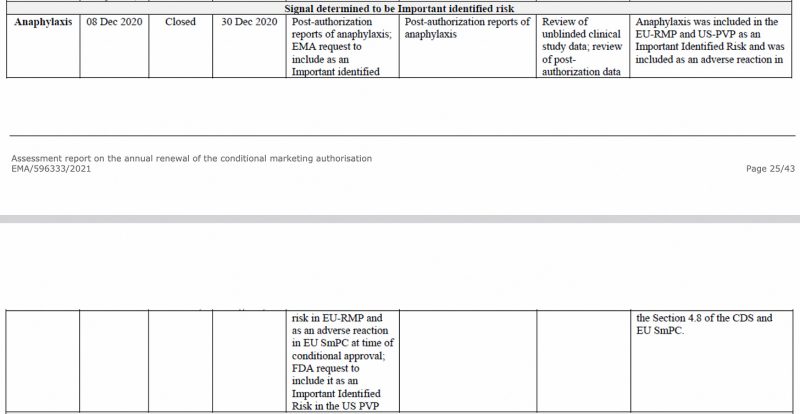
Anafylaxe byla již v prosinci 2020 v CHMP (Výboru pro humánní léčivé přípravky) Evropské agentury pro léčivé přípravky identifikována jako důležité riziko. hodnotící zpráva o vakcíně Pfizer-BioNtech COVID-19, viz níže.
Také v první pravidelné aktualizaci bezpečnosti EU Zpráva, který jsem měl dříve analyzoványanafylaxe byla opět označena jako významné identifikované riziko.

V této zprávě o farmakovigilanci bylo z údajů po registraci identifikováno 3,827 XNUMX relevantních případů (jednotlivců). Zemí s nejvyšším výskytem bylo Japonsko, následované USA a Velkou Británií.
Nejvíce hlášených případů bylo u žen, šokujících 3,182 454 případů oproti 44 případům u mužů, s mediánem věku 7 let. Skutečnost, že 2021krát více případů bylo hlášeno u žen, není žádnou novinkou. Ještě v prosinci XNUMX I analyzovány společnost Pfizer připravila dokument pro FDA na období 3 měsíců od prosince 2020 do 28. února 2021 – v případě anafylaxe byly ženy postiženy 8krát více.
Takže 98 procent relevantních nežádoucích účinků (včetně anafylaktické reakce, anafylaktického šoku, anafylaktoidní reakce a anafylaktoidního šoku) bylo klasifikováno jako závažné!
Navíc u 92 procent případů byla doba, která uplynula, než došlo k nežádoucí události po podání vakcíny, kratší než 24 hodin.

Smrtelné následky
Z 3,922 28 událostí bylo 704 smrtelných a u ohromujících XNUMX byl výsledek neznámý. Nebyla uvedena žádná čísla případů pro smrtelné následky.

Případy podle věkových skupin
Z 3,827 23 relevantních případů (jednotlivců) bylo 3,021 z dětské věkové skupiny a XNUMX XNUMX z věkové skupiny dospělých.
Přítomnost komorbidit
Pozoruhodné je, že se tak stalo zhruba u 2/3 všech případů anafylaxe ne máte nějaké komorbidity (základní zdravotní problémy).

Vzhledem k tomu, co se stalo od uvedení vakcín mRNA COVID-19 na trh, není překvapením číst: “nebyly zjištěny žádné nové bezpečnostní informace týkající se rizika anafylaxe s BNT162b2” (vakcína Pfizer-BioNTech COVID-19). Uvedený důvod (nebo výmluva, za kterou se skrývají) je, že „toto riziko je sděleno..., což zahrnuje informace o vhodných opatřeních, která je třeba podniknout, a to následovně: „Stejně jako u všech injekčních vakcín musí být vždy okamžitě k dispozici vhodná lékařská péče a dohled. v případě vzácné anafylaktické příhody po podání vakcíny.“
Pod Pravidlo 174, Informace pro britské zdravotnické odborníky, který byl naposledy revidován v prosinci 2021, je uvedeno:

ve skutečnosti, na velmi první den o zavedení vakcíny Pfizer-BioNtech COVID-19 ve Spojeném království byly dvě zprávy o anafylaxi a jeden hlášený případ možné alergické reakce. To nezabránilo MHRA ve stažení produktu – jednoduše se tomuto problému vyhnuli prohlášením, že lidé, kteří mají v anamnéze alergie, by vakcínu neměli užívat.
I když věděli – složky lipidových nanočástic ALC-0159 a ALC-0315 od společnosti Pfizer/BioNTech nebyly nikdy předtím obsaženy v žádném licencovaném léku. ALC-0159 obsahuje PEG (polyethylenglykol), který je je známo, že způsobuje anafylaxi.
Je to jednoznačné: anafylaxe byla známá život ohrožující nežádoucí příhoda, přibližně ve stejnou dobu bylo uděleno povolení k nouzovému použití vakcíny Pfizer-BioNtech COVID-19. Přesto, protože se jedná o „injikovatelnou vakcínu“, nějakým způsobem získala povolení od všech regulátorů léčiv, bez ohledu na to, jak mnoho usvědčujících dat se hromadí, když je sirup proti kašli nebo kapsle na druhé straně naléhavě stažen na základě „a velmi vzácné riziko anafylaxe."
Znovu publikováno od autora Náhradník
Publikováno pod a Mezinárodní licence Creative Commons Attribution 4.0
Pro dotisky nastavte kanonický odkaz zpět na originál Brownstone Institute Článek a autor.









